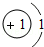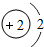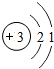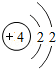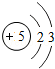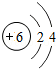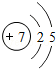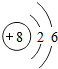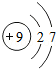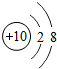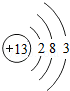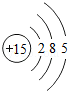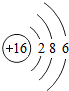四、(本题包括2小题,共15分)
23.(8分)(2013•南京)现有八种物质,选择相应物质的字母填空:
A、活性炭 B、酒精 C、熟石灰 D、聚乙烯塑料
E、钛合金 F、石墨 G、小苏打 H、一氧化碳
(1) D 可用于制食品包装袋 (2) F 可用于制铅笔芯
(3) E 可用于制造人造骨 (4) C 可用于改良酸性土壤
(5) A 可用于吸附冰箱内的异味 (6) H 是有毒气体
(7) G 是发酵粉的主要成分之一 (8) B 是实验室最常用的燃料.
考点: 塑料及其应用;一氧化碳的毒性;合金与合金的性质;常见碱的特性和用途;常用盐的用途;甲烷、乙醇等常见有机物的性质和用途;碳单质的物理性质及用途.
专题: 物质的性质与用途.
分析: 物质的性质决定物质的用途,聚乙烯塑料可用于制食品包装袋;石墨很软;钛合金与人体有很好的相容性;氢氧化钙具有碱性,属于碱,可用于改良酸性土壤;活性炭具有吸附性,能吸附异味和色素;一氧化碳有毒;碳酸氢钠是发酵粉的主要成分之一;酒精具有可燃性;据此进行分析解答.
解答: 解:(1)聚乙烯塑料可用于制食品包装袋.
(2)石墨很软,可用于制铅笔芯.
(3)钛合金与人体有很好的相容性,可用于制造人造骨.
(4)熟石灰是氢氧化钙的俗称,氢氧化钙具有碱性,属于碱,可用于改良酸性土壤.
(5)活性炭具有吸附性,能吸附异味和色素,可用于吸附冰箱内的异味.
(6)一氧化碳有毒,能与血液中的血红蛋白结合使人中毒.
(7)小苏打是碳酸氢钠的俗称,碳酸氢钠是发酵粉的主要成分之一.
(8)酒精具有可燃性,是实验室最常用的燃料.
故答案为:(1)D;(2)F;(3)E;(4)C;(5)A;(6)H;(7)G;(8)B.
点评: 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.
24.(7分)(2013•南京)2013年6月5日是“世界环境日”,中国主题为“同呼吸 共奋斗”.
(1)化石燃料是不可再生能源,包括煤、 石油 和天然气等.
(2)下列不属于空气污染物的是 D .
A、二氧化氮 B、二氧化硫 C、PM2.5 D、氮气
(3)二氧化碳是一种温室气体.某化学兴趣小组利用如图所示装置对二氧化碳的性质进行验证:
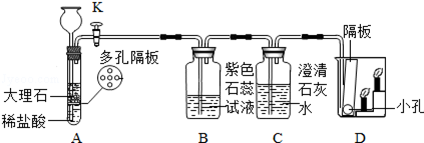
当打开K,反应一段时间后:
①D烧杯中 下层 (填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质是 密度比空气大 ,具有的化学性质是 不燃烧,不支持燃烧 .
②B处紫色石蕊试液变红色,C处澄清石灰水变浑浊.B处使紫色石蕊溶液变红的物质是 碳酸 ;写出C处发生变化的化学方程式 CO2+Ca(OH)2═CaCO3↓+H2O .
考点: 化石燃料及其综合利用;空气的污染及其危害;二氧化碳的实验室制法;二氧化碳的化学性质.
专题: 综合实验题;化学与能源;空气与水.
分析: 石油、煤、天然气属于化石燃料,氮气是空气中含量最多的物质;
根据实验现象可以判断物质的性质;
显酸性的溶液能使石蕊试液变红色,显碱性的溶液能使石蕊试液变蓝色;
书写化学方程式要注意规范性.
解答: 解:(1)化石燃料是不可再生能源,包括煤、石油和天然气等.
故填:石油.
(2)二氧化氮、二氧化硫和PM2.5 都属于空气污染物,而氮气是空气的主要成分,不是空气污染物.
故填:D.
(3)①当打开K,反应一段时间后,可以观察到下层的蜡烛先熄灭,说明二氧化碳的密度比空气大,不燃烧,不支持燃烧.
故填:下层;密度比空气大;不燃烧,不支持燃烧.
②B处紫色石蕊试液变红色,说明B中有显酸性的物质的生成,显酸性的物质是碳酸,碳酸是由二氧化碳和水反应生成的.
故填:碳酸.
C处澄清石灰水变浑浊,是因为二氧化碳和氢氧化钙反应生成了不溶于水的物质﹣﹣碳酸钙,同时生成水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
故填:CO2+Ca(OH)2═CaCO3↓+H2O.
点评: 本题主要考查了物质的性质和化学方程式的书写,书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”.
五、(本题包括3小题,共16分)
25.(4分)(2013•南京)以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):
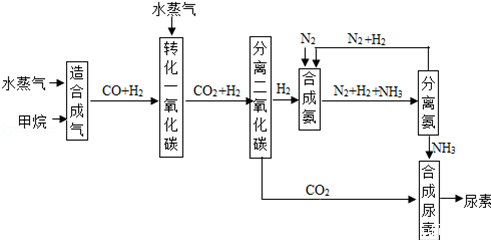
(1)尿素与熟石灰混合研磨 无 (填“有”或“无”)刺激性气味.
(2)甲烷和水蒸气在高温及催化剂的条件下反应,生成CO和H2,该反应的化学方程式为 CH4+H2O CO+3H2 .
CO+3H2 .
(3)分离出氨后,可循环利用的两种物质是 氮气 、 氢气 .
考点: 物质的相互转化和制备.
专题: 物质的制备.
分析: (1)铵根离子与氢氧根离子结合能生成氨气,尿素中没有铵根离子,进行分析;(2)根据方程式的书写方法进行书写;(3)根据生产流程图中所涉及的物质的来源和去向回答.
解答: 解:(1)铵根离子与氢氧根离子结合能生成氨气,尿素中没有铵根离子,不能与熟石灰反应生成氨气,所以尿素与熟石灰混合研磨无刺激性气味生成;
(2)反应物是甲烷和水,生成物是一氧化碳和氢气,用观察法配平,反应条件是高温和催化剂,所以方程式是:CH4+H2O CO+3H2;
CO+3H2;
(3)可循环利用的物质是在前面反应中是反应物,在后面的反应中是生成物,分析生产流程图中所涉及的物质的来源和去向发现,N2和H2是循环利用的物质.
故答案为:(1)无;(2)CH4+H2O CO+3H2;(3)氮气;氢气.
CO+3H2;(3)氮气;氢气.
点评: 化学来源于生产、生活,又服务于生产、生活,要知道铵根离子与氢氧根离子结合能生成氨气,熟悉方程式的书写方法.
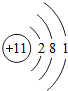
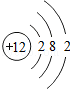
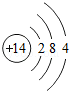
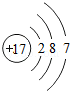
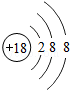
26.(7分)(2013•南京)核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
第一周期 | 1H | 2He | ||||||
第二周期 | 3Li | 4Be | 5B | 6C | 7N | 8O | 9F | 10Ne |
第三周期 | 11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar |
(1)在第三周期中,各原子结构的共同之处是 各原子的电子层数相同 ;该周期中,各原子核外电子排布的变化规律是 最外层电子数依次递增 .
(2)在第三周期中,元素类型的变化情况是:从左到右由 金属 元素过渡到 非金属 元素,并以稀有气体元素结尾.
(3)写出核外电子排布与氖原子形同的阳离子和阴离子符号各一个:阳离子 Na+ ,阴离子 O2﹣ .
(4)写出含有氮元素的常见氧化物、酸、碱、盐的化学式各一个:
物质的类别 | 氧化物 | 酸 | 碱 | 盐 |
物质的化学式 | NO2 | HNO3 | NH3•H2O | NH4NO3 |
考点: 元素周期表的特点及其应用;化学式的书写及意义;化学符号及其周围数字的意义.
专题: 化学用语和质量守恒定律.
分析: (1)第三周期各原子电子层数都是3层;根据原子结构示意图中最外层电子数的变化关系考虑;
(2)根据最外层电子数小于4的一般是金属元素,最外层电子数多于或等于4属于非金属;
(3)阳离子是带正电荷,阴离子是带负电荷,电子数等于10个就行;
(4)根据化学式的写法,氧化物是由两种元素组成,一种元素是氧元素的化合物,酸是电离出的阳离子都是氢离子的化合物,电离出金属离子(或铵根离子)和酸根离子的化合物属于盐,氨水属于碱.
解答: 解:(1)元素的周期数与原子的核外电子层数相同.第三周期各原子电子层数都是3层;原子结构示意图中最外层电子数由左向右依次递增;
(2)最外层电子数小于4的一般是金属元素,最外层电子数多于或等于4属于非金属,汉字中带钅字旁的属于金属元素(金和汞除外);由图示可知从左到右由金属元素过渡到非金属元素;
(3)氖原子是10个电子,阳离子是带正电荷,阴离子是带负电荷,所以钠离子属于阳离子,核外电子数是10个,符号为:Na+;氧离子带2个单位负电荷,属于阴离子,核外电子数也是10个;符号是O2﹣;
(4)氧化物是由两种元素组成,一种元素是氧元素的化合物,所以二氧化氮属于氧化物,化学式是NO2;酸是电离出的阳离子都是氢离子的化合物,硝酸就是酸,化学式是:HNO3;氨水属于弱碱,化学式是NH3•H2O;带铵根的盐属于铵盐,所以硝酸铵属于盐,化学式是NH4NO3.
故答案为:(1)各原子的电子层数相同;最外层电子数依次递增;(2)金属;非金属;(3)Na+;O2﹣;(4)
物质的类别 氧化物 酸 碱 盐
物质的化学式 NO2 HNO3 NH3•H2O NH4NO3
点评: 本题考查学生对原子结构示意图、元素周期律知识的理解与在解题中灵活应用的能力.
27.(5分)(2013•南京)下图中的A~I表示几种初中化学常见的物质,其中A、D、I是氧化物,I中两种元素质量之比为3:4;B元素在地壳中的含量位居第三;C由三种元素组成;G为紫红色.图中“﹣”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
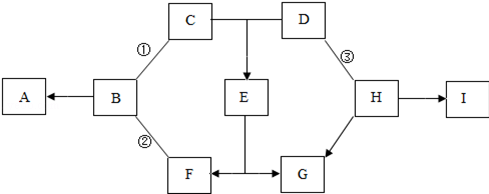
(1)写出G的化学式 Cu ;E的化学式 CuSO4 .
(2)写出B→A反应的化学方程式 4Al+3O2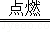 2Al2O3 .
2Al2O3 .
(3)反应①、②和③的基本反应类型相同,该基本反应类型是 置换反应 .
(4)写出H与D反应的化学方程式 2CuO+C 2Cu+CO2↑ .
2Cu+CO2↑ .
考点: 物质的鉴别、推断.
专题: 框图型推断题.
分析: 本题的突破口是B元素在地壳中的含量位居第三,因此是铝,而B能够转化成A氧化物,因此A是氧化铝;铝还能和C和F反应,因此C和F是酸和盐,C由三种元素组成且能够和D氧化物反应,因此确定C是硫酸,E是盐溶液;F是盐且是排在铝后面的金属形成的盐溶液;G是紫红色的铜,所以E硫酸铜,则D为氧化铜;H能够和氧化铜反应,说明H具有还原性,而I是氧化物,I中两种元素质量之比为3:4,且I是H反应产生的,所以I为一氧化碳,然后带入验证回答问题即可.
解答: 解:B元素在地壳中的含量位居第三,因此是铝,而B能够转化成A氧化物,因此A是氧化铝;铝还能和C和F反应,因此C和F是酸和盐,C由三种元素组成且能够和D氧化物反应,因此确定C是硫酸,E是硫酸盐,F是盐且是排在铝后面的金属形成的盐溶液,如硫酸亚铁;G是紫红色的铜,所以E硫酸铜,则D为氧化铜;H能够和氧化铜反应,说明H具有还原性,而I是氧化物,I中两种元素质量之比为3:4,且I是H反应产生的,所以I为一氧化碳,H是碳.
(1)G为紫红色的铜,E为硫酸铜;故答案为:Cu; CuSO4;
(2)B是铝,A是氧化铝,因此B→A反应的化学方程式为:4Al+3O2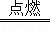 2Al2O3;故答案为:4Al+3O2
2Al2O3;故答案为:4Al+3O2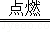 2Al2O3;
2Al2O3;
(3)反应①是硫酸和铝的反应、②是铝和硫酸盐的反应;③是碳和氧化铜的反应,三个反应都是置换反应;故答案为:置换反应;
(4)H是碳与D氧化铜反应的化学方程式为:2CuO+C 2Cu+CO2↑;故答案为:2CuO+C
2Cu+CO2↑;故答案为:2CuO+C 2Cu+CO2↑.
2Cu+CO2↑.
点评: 本题是一个根据常见物质的性质展开的推断题,解决本类题目的关键是找准解题的突破口,然后利用物质的性质正推、逆推、交叉推等途径得出结论,最后带入验证即可.
六、(本题包括1小题,共11分)
28.(11分)(2013•南京)某兴趣小组对物质的性质进行相关探究、
【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:
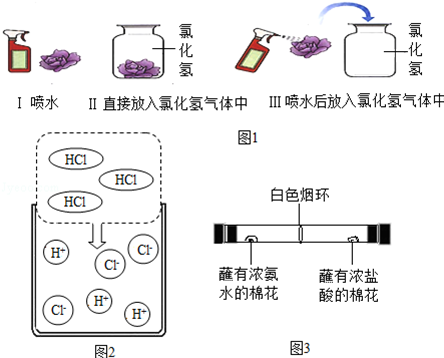
实验现象:Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的示意图.
【实验结论】氯化氢气体不显酸性.
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是 在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性 .
(2)小明向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式 NaOH+HCl=NaCl+H2O .
(3)紫甘蓝的汁液在酸性溶液中显 红 色.
(4)下列实验可以用来说明氯化氢气体不显酸性的是 B .
A、测试盐酸的导电性,盐酸能导电
B、干燥的碳酸钠粉末放入氯化氢气体中,不反应
C、氢气与氯气反应,生成氯化氢气体
D、干燥的碳酸钠粉末放入盐酸中,能反应
【拓展应用】
(1)该兴趣小组的同学为探究分子的运动情况,在玻璃管两端同时放入蘸有试剂的棉花,做了如图3所示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端.
①白色烟环偏向蘸有浓盐酸的棉花一端的原因是 氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端 .
②写出该反应的化学方程式 NH3+HCl=NH4Cl .
(2)氢气在氯气中燃烧生成氯化氢气体,燃烧100g氢气,理论上生成氯化氢气体的质量是多少?(在答题卡上写出计算过程)
考点: 实验探究物质的性质或变化规律.
专题: 科学探究.
分析: 【交流反思】
(1)根据氯化氢气体是由氯化氢分子构成的进行解答;
(2)根据稀氢氧化钠溶液和盐酸反应生成氯化钠和水进行解答;
(3)根据图可知紫甘蓝的汁液在酸性溶液中显红色进行解答;
(4)根据碳酸钠粉末遇到酸性物质会生成二氧化碳进行解答;
【拓展应用】(1)根据氨分子的运动速率大于氯化氢分子的运动速率以及氨气和氯化氢气体反应生成氯化铵固体进行解答;
(2)根据氢气的质量求出生成氯化氢气体的质量即可.
解答: 解:【交流反思】
(1)在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性;故填:在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性;
(2)稀氢氧化钠溶液和盐酸反应生成氯化钠和水,所以向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,反应的化学方程式NaOH+HCl=NaCl+H2O;故填:NaOH+HCl=NaCl+H2O;
(3)由图可知紫甘蓝的汁液在酸性溶液中显红色;故填:红;
(4)碳酸钠粉末遇到酸性物质会生成二氧化碳,所以干燥的碳酸钠粉末放入氯化氢气体中,不反应,说明氯化氢气体不显酸性;故填:B;
【拓展应用】(1)①白色烟环偏向蘸有浓盐酸的棉花一端的原因是:氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端;故填:氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端;
②氨气和氯化氢气体反应生成氯化铵固体,该反应的化学方程式NH3+HCl=NH4Cl;故填:NH3+HCl=NH4Cl;
(2)设生成氯化氢气体的质量是x
H2+Cl2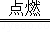 2HCl
2HCl
2 73
100g x
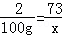
x=3650g
答:生成氯化氢气体的质量是3650g.
点评: 此题重点考查了碱与二氧化碳反应的性质,以及分子的运动知识,是中考的热点内容之一.