五、(本题包括3小题,共17分)
25.开发氢能源是实现社会可持续发展的需要.
工业上可用煅烧黄金矿(主要成分FeS2)产生的二氧化硫通过下列工艺过程制取氢气.
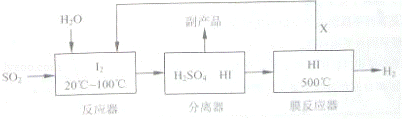
(1)写出膜反应器中HI气体发生分解反应的化学方程式 ;
(2)分离器中分离出的副产品是 ,生产流程中能被循环利用的物质X为 。
【答案】 (1)2HI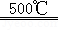 H2+I2(2)硫酸 I2
H2+I2(2)硫酸 I2
【解析】(1)由题意知,HI气体发生分解反应生成碘和氢气,反应的化学方程式为:2HI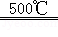 H2+I2;
H2+I2;
(2)由工艺流程图中可以看到分离器中分离出的副产品是硫酸,生产流程中能被循环利用的物质是I2。
【点评】 本题必须通过题中图示找出一些信息,找出物质间的相互转换,本题难度不大,贵在学会分析图象。
26.根据初中化学所学知识回答下列问题:
(1)判断稀盐酸与下表中的四种化合物溶液之间能否发生反应.请仿照示例,在表格内②③④处填写(“能”或“不能”)
,并根据复分解反应发生的具体条件在对应的表格中填写判断依据.
氢氧化钠溶液 | 氯化钠溶液 | 碳酸钾溶液 | 硝酸银溶液 | |
稀盐酸 | 示例:① 反应 | ② 反应 | ③ 反应 | ④ 反应 |
判断依据 | 示例: |
(3)某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中残余的硫酸,共消耗氢氧化钠溶液80.0g,洗涤后的溶液呈中性,这一定量石油产品中含H2SO4的质量是多少?
【答案】(1)① 能;有水生成;②不能;无沉淀或无水或无气体生成;③能;有气体生成;④能;有沉淀生成;(2)干燥;2NaOH+CO2═Na2CO3+H2O(3)19.6g
【解析】(1)①稀盐酸与氢氧化钠生成水,满足复分解反应的条件;②稀盐酸和氯化钠,既无沉淀、也无水、也无气体产生,不能发生复分解反应;③稀盐酸和碳酸钾反应生成二氧化碳气体,符号复分解反应的条件;④稀盐酸和硝酸银反应生成氯化银沉淀,符号复分解反应的条件;(2)氢氧化钠能吸收空气中的水而潮解,所以可用作干燥剂;氢氧化钠和空气中的二氧化碳反应生成碳酸钠和水而变质,最终生成碳酸钠。
(3)消耗的氢氧化钠溶液中溶质的质量为:80g×20%=16g
设一定量石油产品里含H2SO4的质量为x
2NaOH+H2SO4=Na2SO4+H2O
80 98
16g x
80:98=16g:x
x=19.6g
答:这一定量的石油产品里含硫酸的质量为19.6g。
【点评】 本道考查了复分解反应的发生的条件,氢氧化钠的性质以及根据 化学方程式的计算,难度不大,但基础知识要扎实。
化学方程式的计算,难度不大,但基础知识要扎实。
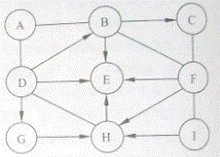
27.如图中的A~I表示几种初中化学常见的纯净物,且分别是由H、C、O、S、Cl、Na、Ca中的两种或两种以上元素组成.其中A、E、H是氧化物;A中氧元素质量分数为60%;I俗称小苏打,C、I分别与足量F反应的生成物相同.图中“﹣”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物或生成物已略去.
(1)写出I的化学式 ;E的化学式 。
(2)在C物质的水溶液中滴加无色酚酞溶液,酚酞溶液显 色.
(3)写出A和B反应的化学方程式 。
(4)写出G发生分解反应的化学方程式 。
【答案】(1)NaHCO3; H2O.(2)红.(3)SO3+2NaOH=Na2SO4+H2O(4)CaCO3 CaO+CO2↑.
CaO+CO2↑.
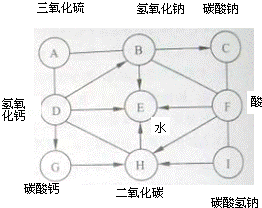
【解析】 由于I为小苏打,所以为碳酸氢钠,而C和F反应产物和I与F反应产物相同,说明C为碳酸钠.而A为氧化物,且氧元素为60%,根据给定元素可以推断应该是三氧化硫.由于B与A反应,说明B 为碱.而B能够转化为C(碳酸钠),且D为碱,也能转化为B,所以B为碱,为氢氧化钠.碳酸钠和碳酸氢钠以及氢氧化钠都能和F反应,则F为酸(盐酸、硫酸均可).而碳酸氢钠能够转化为H,H为氧化物,所以为二氧化碳或者是水,而D确定是碱,所以为氢氧化钙,G为碳酸钙.而E为水。
(1)I为碳酸氢钠,由于钠元素为+1价,而碳酸氢根为﹣1价,根据化合物中化合价的代数和为零可得其化学式 NaHCO3;E的化学式 H2O。
(2)C为碳酸钠,其水溶液显碱性,所以滴加无色酚酞溶液,酚酞溶液显红色。
(3)A(三氧化硫)和B(氢氧化钠)反应得到硫酸钠和水,其化学方程式 SO3+2NaOH=Na2SO4+H2O。
(4)写出G发生分解反应的化学方程式 CaCO3 CaO+CO2↑。
CaO+CO2↑。
【点评】 从整体把握,从给定元素对应化合物去试探对号入座,这也是物质推断的一个技巧。
六、(本题包括1小题,共9分)
28.钢铁工业是国家工业的基础.
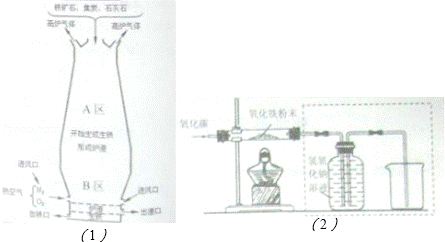
(1)如图1是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.
若图中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:
A区 Fe2O3+3CO 2Fe+3CO2 .
2Fe+3CO2 .
B区 C+O2 CO2,CO2+C
CO2,CO2+C 2CO .
2CO .
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
【设计实验】
用一氧化碳还原纯净的氧化铁粉末,实验装置如图2.
【进行实验】
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【分析与讨论】
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提 出了质疑,于是大家
出了质疑,于是大家
提出查阅资料.
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
③
物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
颜色 | 黑色 | 黑色 | 红色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和 。
②进行猜想:黑色固体粉末可能
a.全部为铁 b. c.
【得出结论】
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称) 。
【反思与评价】
①一氧化碳还原氧化铁的实验中 ,若要得到铁可适当提高反应温度和延长反应时间.
,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有 。
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.

【得出结论】依据实验测得的数据可知氧化铁的质量是:66g﹣60g=6g,这些氧化铁中含有的氧元素质量是:6g×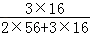 ×100%=1.8g,由于反应前后固体的质量差即为氧化铁失掉的氧的质量,所以可知反应前后失掉的氧的质量是:66g﹣65.2g=0.8g,所以该固体不可能全是铁,固体中还有1g氧元素没有失掉,假设全是四氧化三铁则其含有的氧元素质量是:5.2g×
×100%=1.8g,由于反应前后固体的质量差即为氧化铁失掉的氧的质量,所以可知反应前后失掉的氧的质量是:66g﹣65.2g=0.8g,所以该固体不可能全是铁,固体中还有1g氧元素没有失掉,假设全是四氧化三铁则其含有的氧元素质量是:5.2g×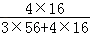 ×100%≈1.43g,故不可能全部是四氧化三铁,所以该固体粉末是铁与四氧化三铁的混合物;
×100%≈1.43g,故不可能全部是四氧化三铁,所以该固体粉末是铁与四氧化三铁的混合物;
【反思与评价】因为二氧化碳和氢氧化钠溶液能反应且无现象,一氧化碳不能与氢氧化钠反应;
A、由于一氧化碳不能与氢氧化钠反应,结合装置的特点可知该装置能收集一氧化碳, 同时排出氢氧化钠溶液; B、二氧化碳和氢氧化钠溶液能反应,所以可以用来吸收二氧化碳; C、由于二氧化碳和氢氧化钠溶液反应时没有明显的现象产生,所以不能用它来检验二氧化碳
同时排出氢氧化钠溶液; B、二氧化碳和氢氧化钠溶液能反应,所以可以用来吸收二氧化碳; C、由于二氧化碳和氢氧化钠溶液反应时没有明显的现象产生,所以不能用它来检验二氧化碳 的存在。
的存在。
【点评】 此题是与炼铁相关的实验探究题,综合性较强,尤其是利用数据对混合物的判断提高了试题的难度,只要是掌握固体质量变化是氧元素失掉的实质便可迎刃而解。











