三、简答题(每空1分,化学方程式2分,共12分)
13.北方的冬天,人们多以煤来提供热量,请结合所学知识回答下列问题:
(1)从燃烧的条件分析,煤属于 ;
(2)煤燃烧时会产生能形成酸雨的气体,如 (填一种物质即可),它能对环境造成污染。
14.根据下列结构示意图,请回答问题:
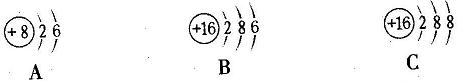
(1)A表示的粒子属于——元素(选填“金属”或“非金属”);
(2)化学性质相似的粒子是——(填字母);
(3)在化学反应中可以相互转化的粒子是——(填字母)。
15.以下是探究Cu、Fe、Ag三种金属活动性顺序的实验过程,请回答问题:
(1)将铜丝和铁丝分别放入相同浓度的稀H2SO4中,依据现象,证明Fe的活动性比Cu强;
(2)将铜丝放入AgNO3溶液中,或向Cu(NO3)2溶液中放入金属,都能证明Cu的活动性比Ag强。
结论:三种金属的活动性顺序是Fe>Cu>Ag
Cu与AgNO3溶液反应的化学方程式为。
16.根据化学反应方程式:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,请回答下列问题:
(1)该反应所属的基本反应类型是;
(2)若上述两种溶液恰好完全反应,反应后的溶液中除水之外,还含有的物质是;
(3)反应后溶液的总质量比反应前溶液的总质量。
四、实验与探究题(每空1 分,化学方程式2分,
分,化学方程式2分, 共12分)
共12分)
17.依据下列装置示意图,请回答问题:
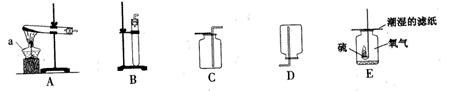
(1)仪器a的名称是 ;
(2)用MnO2催化H2O2溶液制取氧气,应选择的发生 和收集装置是
和收集装置是 (填字母),反应的化学方程式为;
(填字母),反应的化学方程式为;
(3)装置E中,潮湿的滤纸起到的作用是 。
18。某研究性学 习小组将CaCO3与HCl反应后的废物进行处理,目的是制取中性干燥剂CaCl2。得到固体后,他们对固体的成分进行了如下探究:
习小组将CaCO3与HCl反应后的废物进行处理,目的是制取中性干燥剂CaCl2。得到固体后,他们对固体的成分进行了如下探究:
[提出猜想]
猜想一:只有CaCl2
猜想二:CaCl2和CaCO3
猜想三:CaCl2和HCl
通过讨论,大家认为“猜想三”不成立,理由是。
[实验探究]
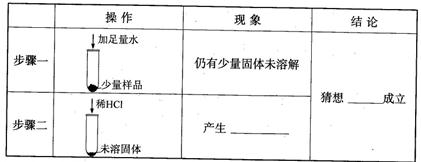
(1)写出有关反应的化学方程式:
(2)实验结束后,同学们根据复分解反应发生的条件,总结出得到CaCl2的不同途 径,
径,
如:①Ca(OH)2+YCln→CaCl2+Z↓,那么Z可能是(填一种即可);
②CaXm+ YCln →CaCl2+H2O,则“YCln”属于类物质。
五、计算题(共6分)
19.质量分数为20%的氢氧化钠溶液40g与一定质量的稀盐酸恰好完全反应,请计算:
(1)生成氯化钠的质量是多少?
(2)若所 用稀盐酸的质量为60g,则所得氯化钠溶液的质量分数为——。
用稀盐酸的质量为60g,则所得氯化钠溶液的质量分数为——。











